在肿瘤精准治疗领域,抗体药物偶联物(ADC)的研发始终聚焦于“增效减毒”,其独特的“抗体靶向识别+毒素高效杀伤”模式,使其成为近年来生物医药领域的研究热点。然而,ADC研发过程中的核心技术瓶颈,长期阻碍着其临床转化与疗效提升——抗体分子的水溶性与肿瘤杀伤毒素(payload)的疏水性之间存在天然冲突,这直接引发高载药比例的ADC易聚集、体内循环稳定性差等问题,限制了其临床应用价值。
针对这一关键难题,南方科技大学王鹏教授和吴奎教授团队在《Journal of Controlled Release》期刊发表综述性研究,系统阐述了ADC亲水连接子(hydrophilic linkers)的设计原理、分类特征、作用机制及最新研究进展,为突破上述瓶颈提供了系统的理论支撑与实践指导。

亲水连接子的核心定位:ADC精准递送的“关键调控者”
ADC的分子结构由抗体、连接子与毒素三部分构成,其中连接子并非简单的“连接桥梁”,而是决定ADC体内代谢命运、调控疗效与毒性的核心组件。
其核心功能主要体现在两个方面:一是维持ADC在血液循环中的结构稳定性,防止毒素提前脱落引发脱靶毒性;二是在ADC被肿瘤细胞内吞后,高效释放毒素,确保肿瘤杀伤的特异性与有效性。
当前抗体药物偶联物(ADC)研发面临的主要困境,均与连接子及毒素的疏水性紧密相关:当提高药物抗体比(DAR)以增强杀伤效能时,疏水性毒素与连接子的累积会致使ADC分子间作用力增大,进而引发聚集现象,这不仅会降低药物疗效,还可能诱发机体免疫反应;同时,疏水性连接子在血液循环中易被酶降解,导致毒素提前脱落,从而造成骨髓抑制、肺损伤等脱靶毒性。
而引入亲水连接子是解决上述困境的关键策略——通过在连接子分子中引入亲水基团,能够有效平衡ADC整体的亲疏水性。一方面可提高高载药ADC的水溶性,减少分子聚集;另一方面可增强ADC在体内的循环稳定性,优化药代动力学特性,最终达成“提升疗效、降低毒性”的研发目标,这亦是各类亲水连接子研究的核心出发点。
主流亲水连接子类型:特性、优势与研究进展
该综述根据亲水连接子的分子结构与作用特征,将其划分为四大主流类型,各类连接子在设计逻辑、性能优势及临床转化潜力上存在显著差异。
(一)聚乙二醇(PEG)类:传统成熟型亲水连接子
聚乙二醇(PEG)修饰技术是药物递送领域应用最为广泛的亲水修饰手段,其凭借良好的亲水性、生物相容性及化学稳定性,成为ADC亲水连接子中应用最成熟的类型。该类连接子的核心作用机制是通过引入柔性PEG链,增加ADC分子的水溶性,延长其在体内的循环半衰期,同时掩盖毒素的疏水性表面,减少ADC分子间的聚集。
研究表明,PEG的长度、构型(线性或分支)及连接位置,对ADC的整体性能具有决定性影响:
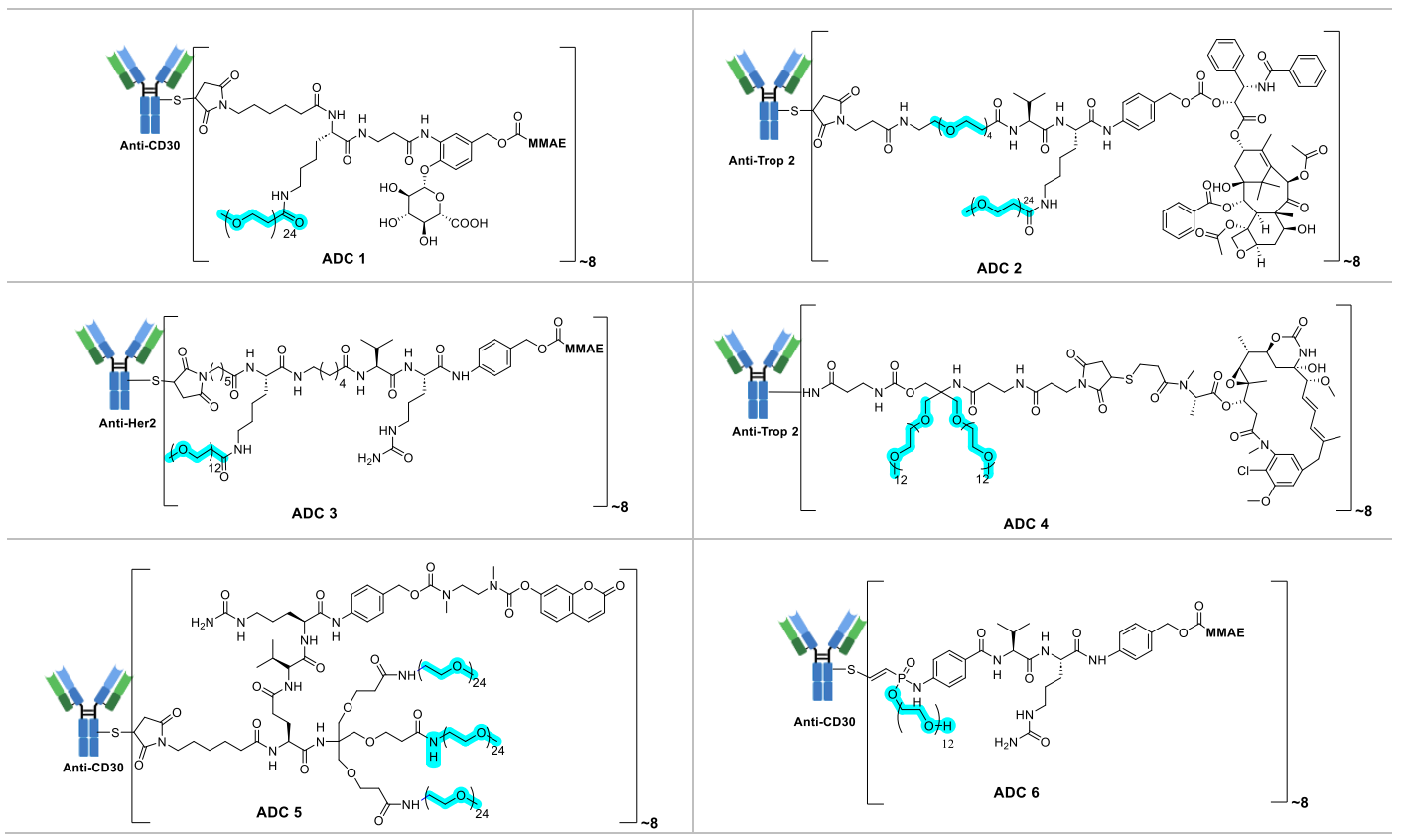
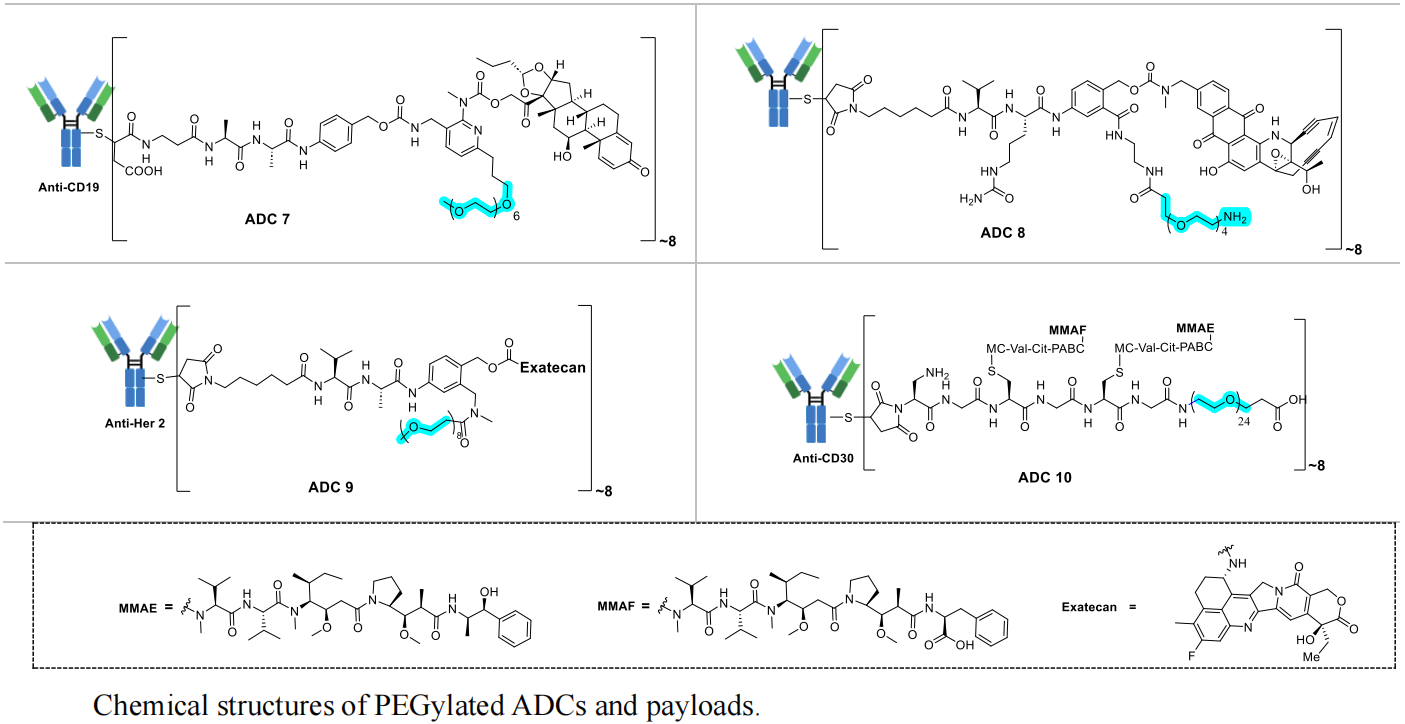
在长度方面,短链PEG(n≤8)可有效改善ADC的水溶性,实现DAR=5~7的高载药比例;在构型方面,分支型PEG相较于线性PEG,能更高效地掩盖毒素的疏水性,减少ADC聚集,同时减慢ADC在体内的清除速度,增强抗肿瘤活性;在连接位置方面,将PEG连接于连接子中部或靠近毒素端,更有利于平衡ADC的亲疏水性,进一步提升其体内稳定性。
尽管PEG类连接子应用成熟,但该综述也指出其存在短板——长期反复给药可能诱导机体产生抗PEG抗体,引发免疫原性反应,导致ADC在体内被加速清除,这一问题也推动了新型亲水连接子的研发。
(二)聚肌氨酸(pSar)类:PEG的新型替代型连接子
为解决PEG类连接子的免疫原性问题,聚肌氨酸(pSar)作为新型亲水聚合物,被广泛探索用于ADC连接子的设计,成为PEG的潜在替代材料。
pSar与PEG具有相当的亲水性与生物相容性,但具备更突出的安全性优势,而作为人体内胆碱代谢的内源性产物,pSar不会引发免疫原性反应,可有效避免抗PEG抗体导致的ADC清除加速问题。
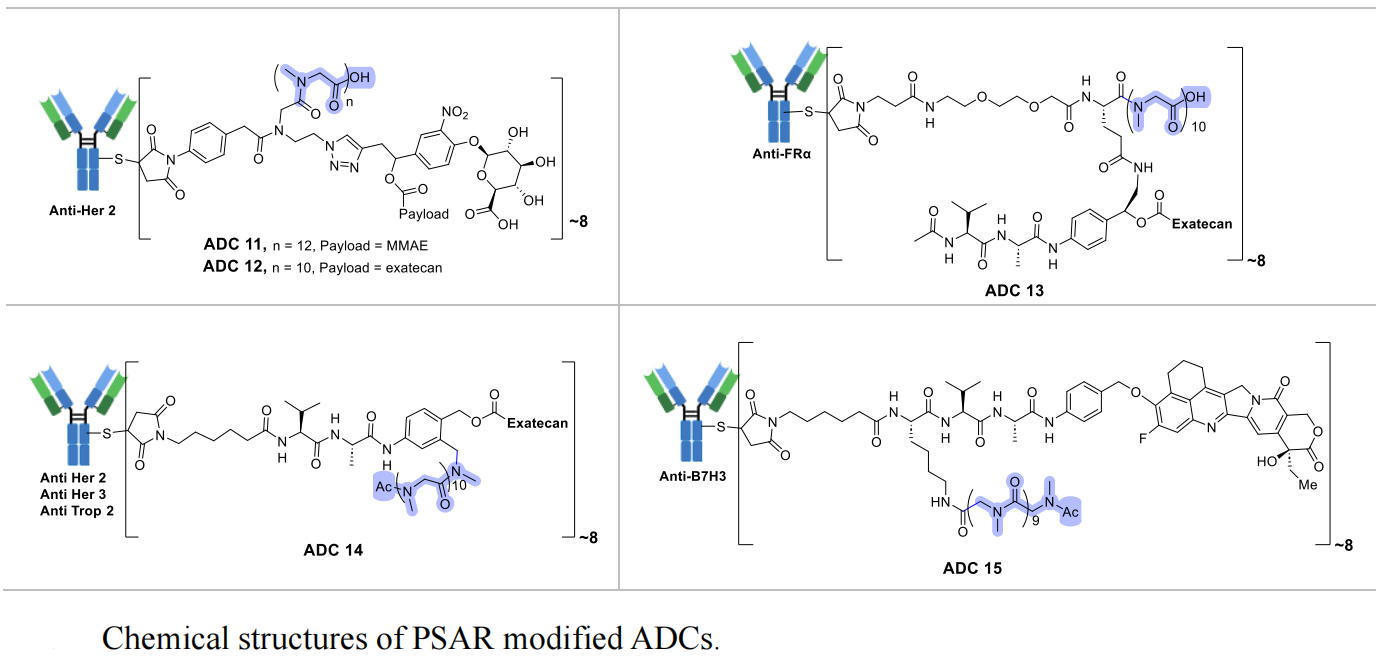
通过与同长度PEG修饰的ADC进行对比研究,综述证实pSar修饰的ADC在性能上具有显著优势:在聚集率方面,pSar₁₀修饰的ADC(ADC 14)聚集率仅为1.16%,远低于同位置PEG₈修饰的ADC(ADC 9,聚集率5.83%),甚至优于临床常用ADC药物DS8201(聚集率5.71%);
在亲水性方面,以ClogP值(疏水性衡量指标,数值越低亲水性越强)为评价标准,pSar₁₀的ClogP=-10.93,显著低于PEG₈的-2.38,可更高效地掩盖毒素的疏水性;在体内疗效方面,pSar₁₂修饰的ADC(ADC 11)抗肿瘤效果优于同长度PEG₁₂修饰的ADC,其中pSar₁₀修饰、DAR=8的MBK-103在动物模型中,即使采用低剂量给药,也能实现高效抗肿瘤作用,且血浆半衰期与天然抗体相当。
与PEG类似,pSar的长度也需要严格选择,该综述表明,pSar₁₀~pSar₁₂是最优长度范围,pSar₂₄虽能进一步提升ADC的稳定性,但过长的分子链会产生空间位阻,阻碍ADC被肿瘤细胞内吞,反而降低疗效。目前,pSar修饰的ADC已进入临床前后期研究,有望成为下一代ADC亲水连接子的主流选择,但仍需解决规模化生产及长期体内安全性验证等问题。
(三)糖类衍生物类:靶向切割型亲水连接子
糖类衍生物具有高生物相容性、可生物降解性及强亲水性等特点,将其引入ADC连接子设计,不仅能实现亲水修饰,还能利用肿瘤细胞内高表达的糖苷酶,实现毒素的肿瘤特异性释放,进一步降低脱靶毒性,是兼具“亲水修饰+靶向切割”双重优势的新型连接子类型。
综述将糖类连接子分为两类,基于不同的设计逻辑实现亲水修饰与毒素释放的协同作用:
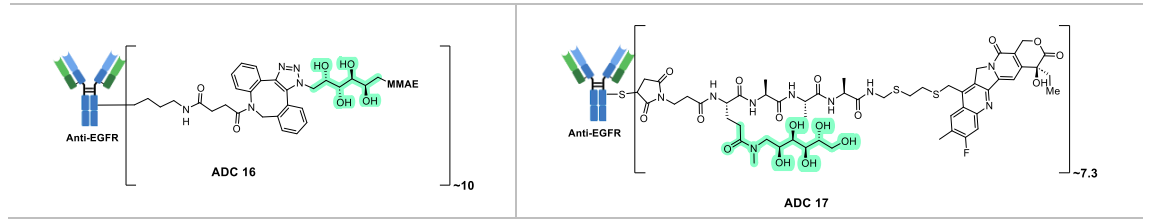
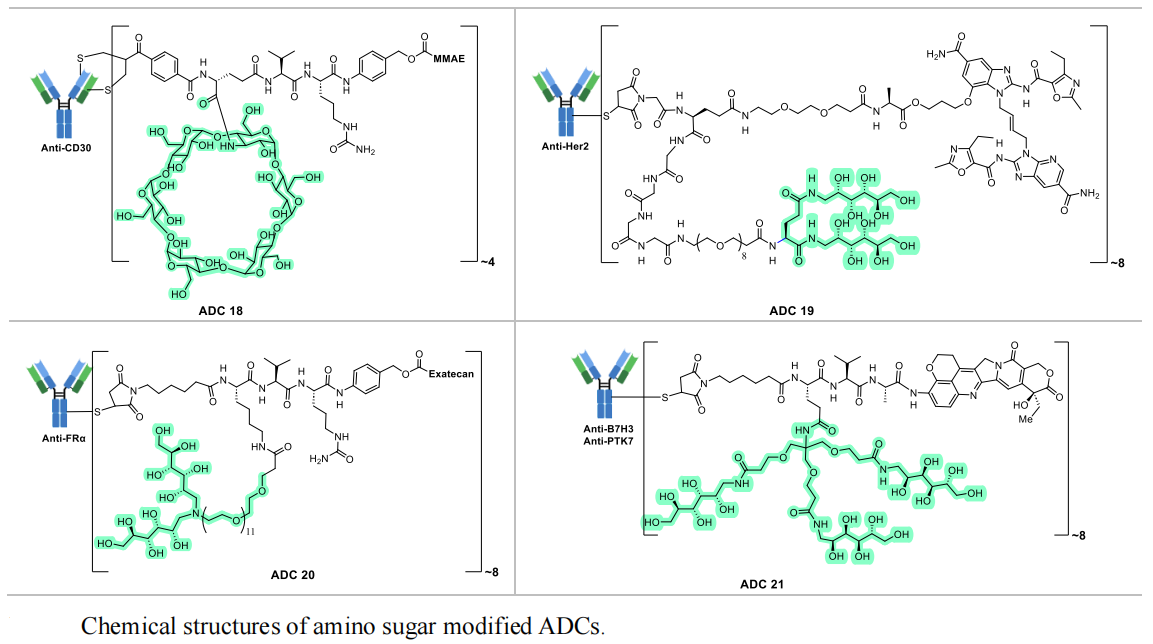
第一类为氨基糖修饰连接子(非切割型):主要通过葡糖胺、环糊精等氨基糖基团的亲水特性,提升ADC的水溶性,助力高载药比例的实现。
第二类为糖苷酶可切割连接子(切割型):其核心设计是利用肿瘤细胞内高表达的β-葡萄糖醛酸酶、β-半乳糖苷酶等,使连接子在肿瘤细胞内被特异性切割,实现毒素的精准释放,避免血液循环中毒素提前脱落。
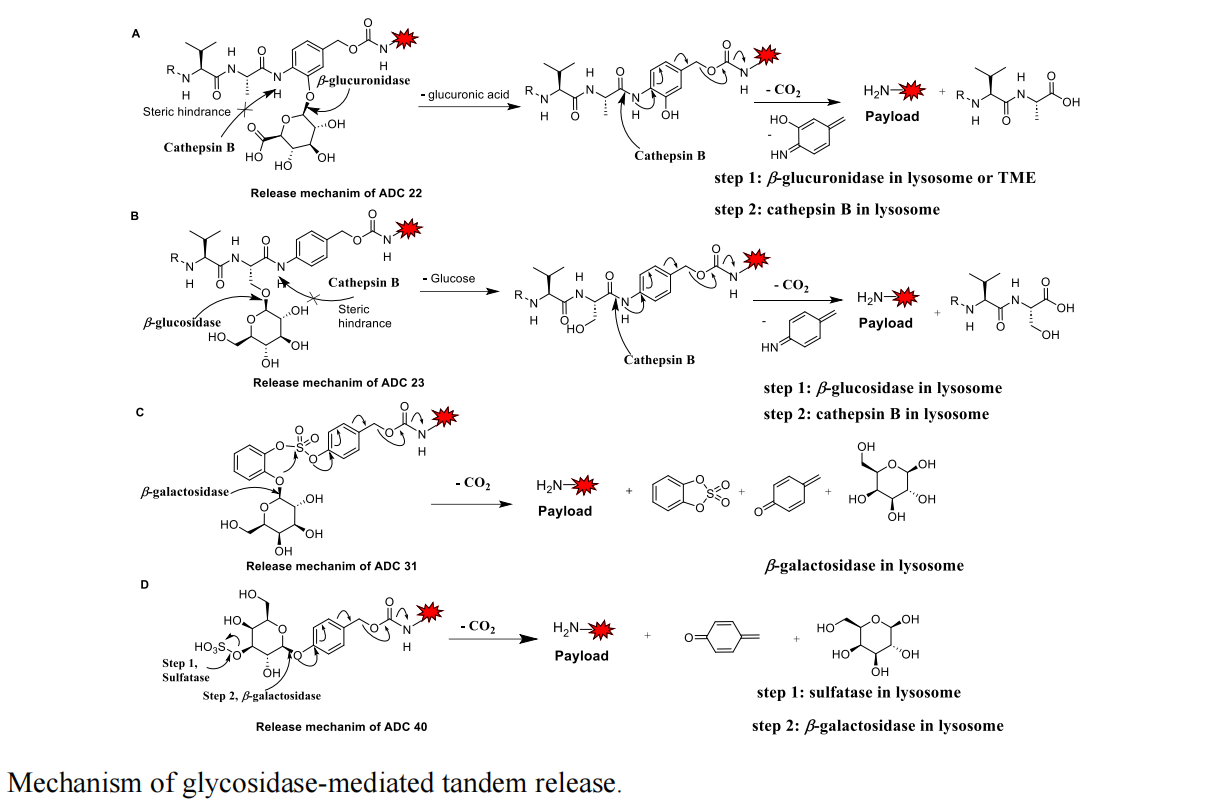
其中,β-葡萄糖醛酸苷连接子是目前研究最成熟的类型,该类连接子在血液循环中可保持结构稳定,进入肿瘤细胞后,被β-葡萄糖醛酸酶特异性切割,释放毒素。
此外,该综述还介绍了α-L-艾杜糖苷、OHPAS支架等新型糖类连接子,这类连接子进一步优化了靶向切割效率与亲水性能,拓展了糖类连接子的应用范围,为实体瘤的精准治疗提供了新的技术思路。
(四)可离子化官能团类:简单高效型亲水连接子
可离子化官能团类亲水连接子的设计逻辑最为简洁直接——通过在连接子分子中引入可离子化基团,利用基团的离子化特性提升ADC的亲水性,同时可通过调控离子化程度,优化毒素的释放动力学,是最经典的亲水修饰策略之一。
综述重点阐述了3类常用可离子化基团修饰的连接子特性及应用进展:
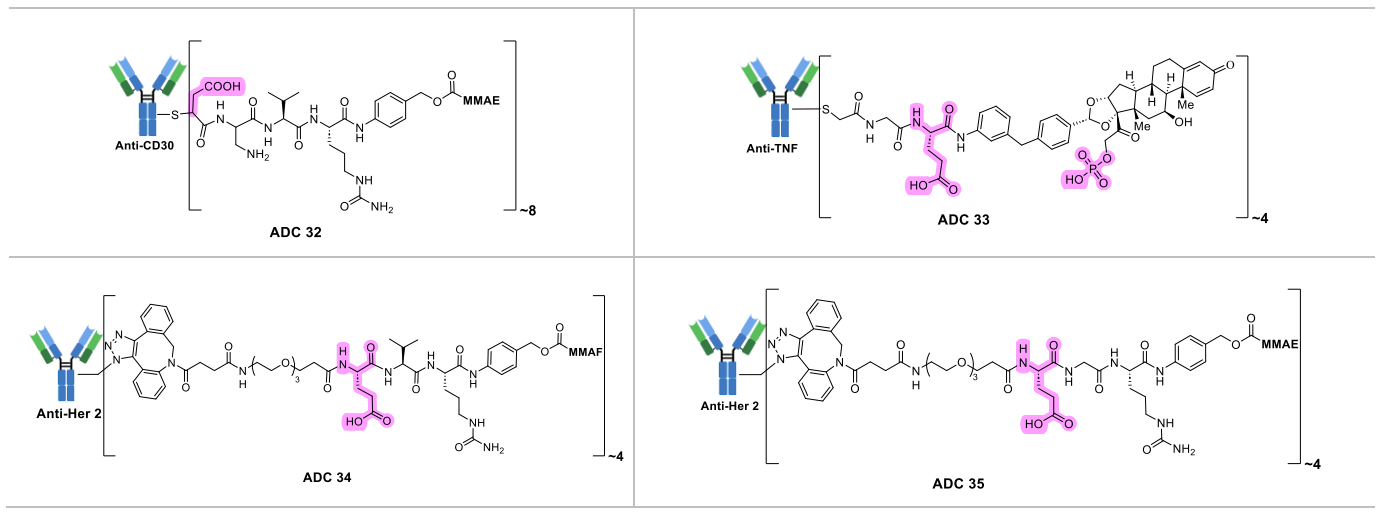
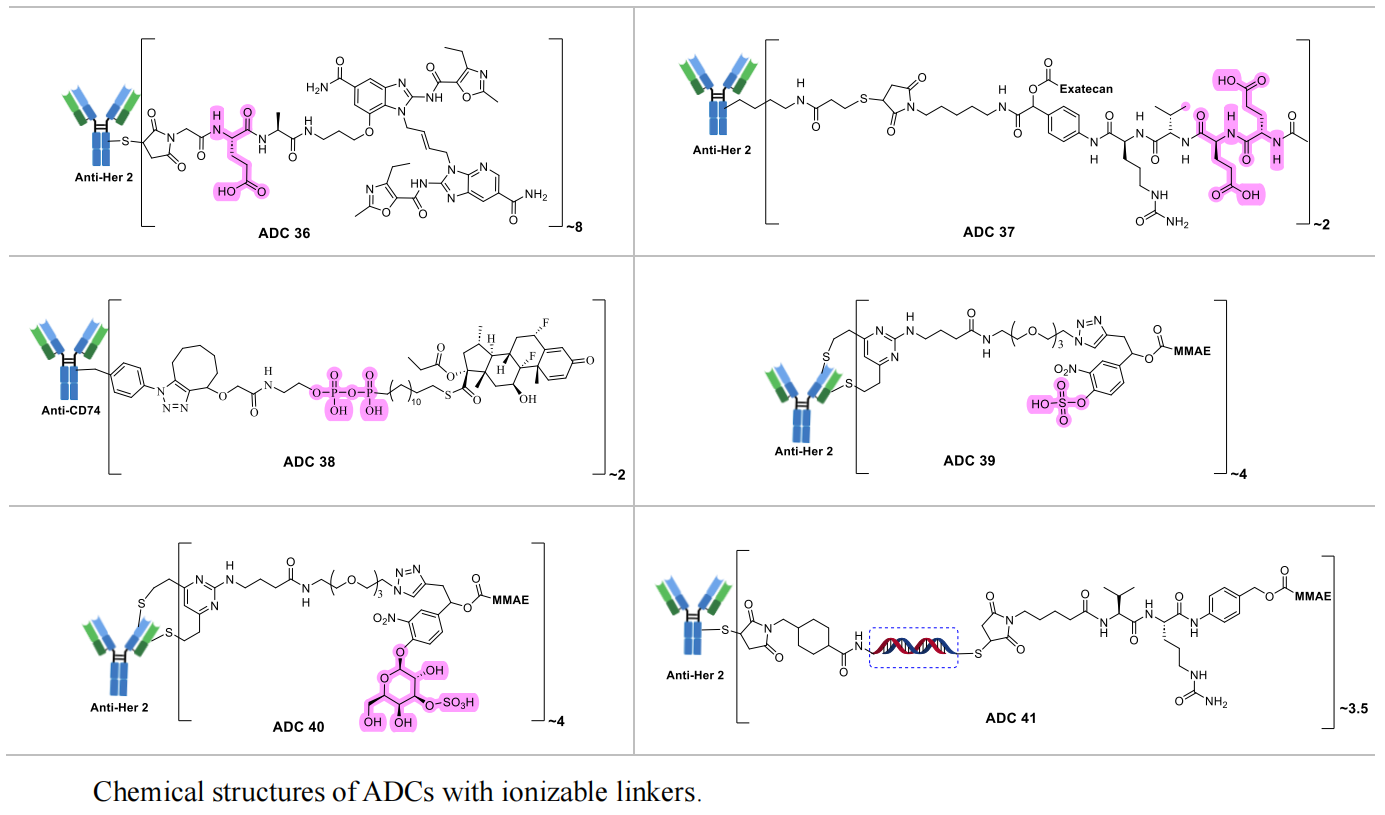
羧酸盐基团(如谷氨酸)是应用最广泛的类型,在连接子中引入谷氨酸(Glu),可显著提升ADC的血浆稳定性,同时保留肿瘤细胞内的酶切活性。
磷酸盐/焦磷酸盐类连接子主要用于解决疏水性类固醇毒素的递送难题,焦磷酸盐作为连接子,既能通过离子化特性提升ADC的水溶性,又能被肿瘤细胞内的磷酸酶特异性切割,实现毒素的快速释放。而非切割型膦酸基团修饰的连接子,则可使毒素局限在肿瘤细胞内,延长其作用时间,进一步提升杀伤效率。
硫酸盐类连接子已实现临床转化,其中sulfo-SPDB连接子修饰的ADC药物Mirvetuximab soravtansine已成功上市,该连接子通过硫酸盐基团的亲水修饰,显著提升了ADC的水溶性与体内稳定性,在FRα阳性卵巢癌治疗中展现出优异的临床效果。
研究总结与未来展望
亲水连接子在ADC研发中的核心价值在于通过平衡ADC分子的亲疏水性,突破高载药比例下的聚集与脱靶毒性瓶颈,实现“高DAR、高稳定性、低毒性”的研发目标。
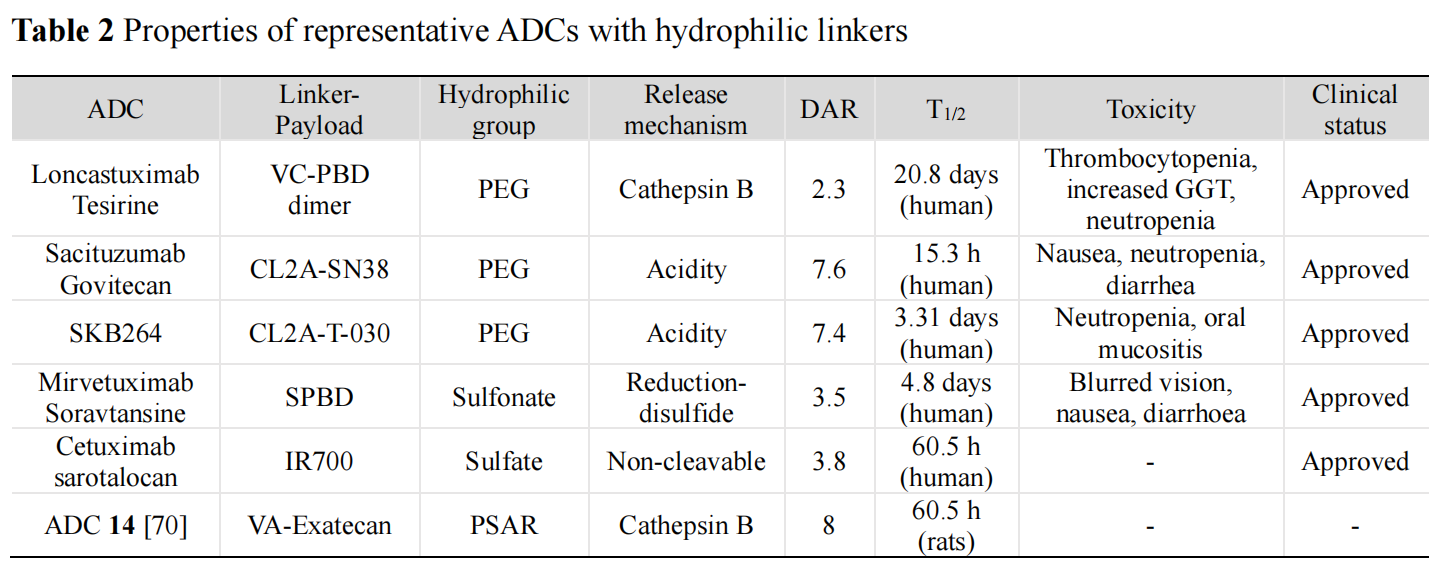
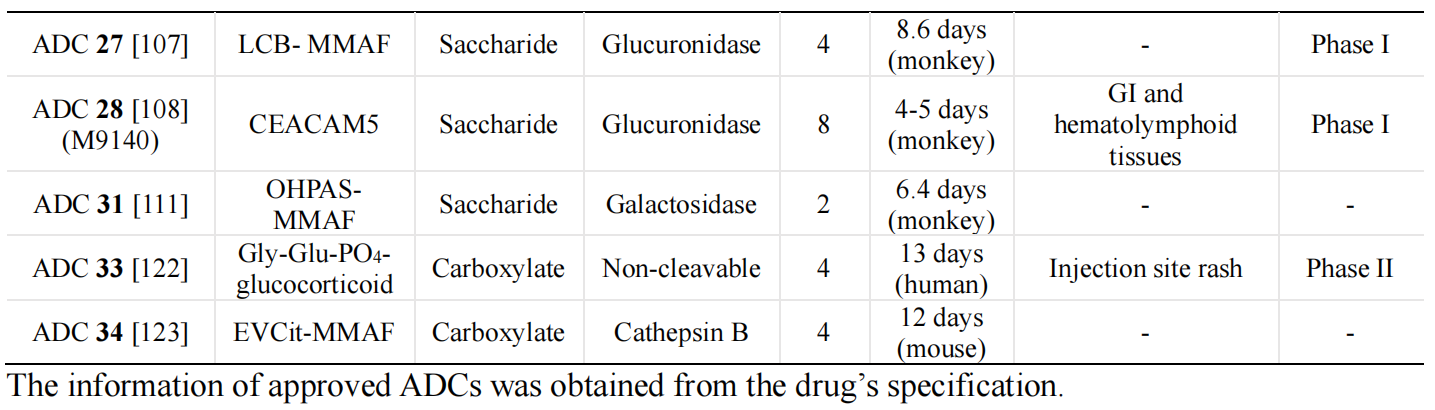
从应用现状来看,PEG类连接子凭借成熟的技术优势,仍是目前临床应用最广泛的类型;pSar类连接子作为PEG的新型替代材料,在性能与安全性上具有显著优势,有望成为下一代主流连接子;糖类衍生物类与可离子化官能团类连接子,分别凭借“靶向切割”与“简单高效”的特点,展现出良好的临床转化潜力。
该综述同时指出,目前亲水连接子的研究仍面临诸多挑战:一是亲水连接子与抗体、毒素的分子匹配性仍需精准优化,不同类型的抗体与毒素需适配特定结构的连接子,才能实现疗效最大化;二是新型亲水聚合物的规模化生产技术尚不完善,制约其临床转化进程;三是亲水连接子的长期体内安全性数据不足,需通过更多临床研究验证其致突变性、致畸性等潜在风险。随着亲水连接子设计技术的不断迭代与优化,以及各类新型连接子的临床研究推进,ADC药物有望进一步突破载药上限与毒性瓶颈,为更多难治性肿瘤患者提供更高效、更安全的治疗方案。
赛诺邦格目前已经成功实现了上述主流亲水连接子(包括PEG类、PSAR类、糖类衍生物类以及可离子化官能团类)的高质量供应。在整个生产与供应的过程中,赛诺邦格凭借一套严格且完善的全流程质量管控体系,对每一个环节都进行了精细的把控,保证了产品的质量与批次稳定性。赛诺邦格为ADC药物的研发与临床转化提供了可靠的核心组件支撑,推动ADC药物在临床应用方面的顺利转化。

Reference:
[1] Fu Q , Kong X , Liu Y ,et al.The role of hydrophilic linkers in next-generation antibody-drug conjugates[J].Journal of Controlled Release, 2026, 391(c):114612.DOI:10.1016/j.jconrel.2026.114612.